Artigo de Ana Pereira | Farmacêutica e Investigadora
A Agência Europeia do Medicamento – EMA- elaborou uma revisão contínua dos agonistas do receptor GLP-1 (agonistas do receptor do peptídeo-1 similar ao glucagon). Estes fármacos são utilizados no tratamento da diabetes tipo 2 (terapêuticas de segunda e terceira linhas como constam nas Recomendações para a Terapêutica Farmacológica da Hiperglicémia na Diabetes Mellitus tipo 2 – Orientações da Comissão Nacional de Farmácia e Terapêutica) sendo também utilizados para a perda de peso, uma vez que se constatou que estes medicamentos conseguem retardar o esvaziamento do estômago, reduzindo o apetite e aumentando e prolongando a sensação de saciedade.
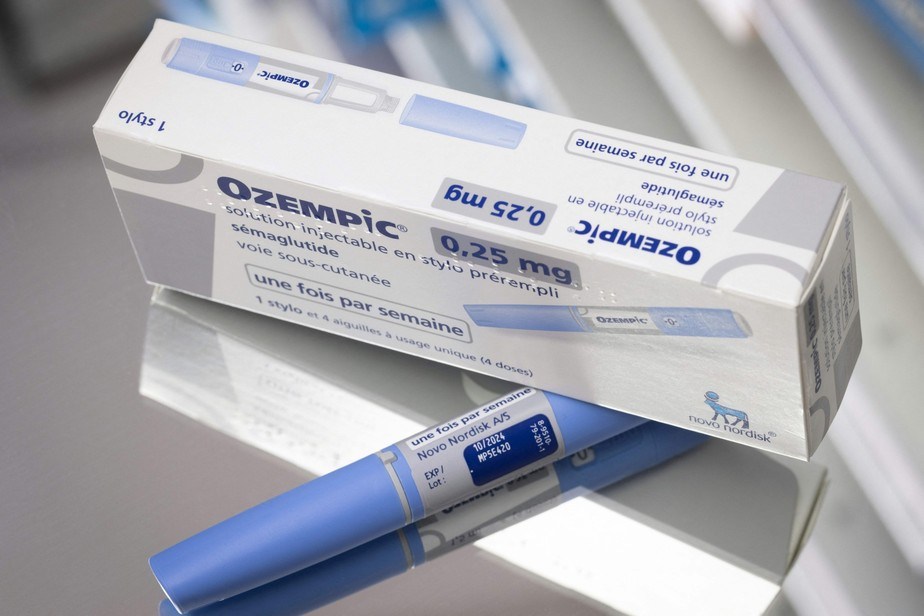
O Comité de Avaliação do Risco em Farmacovigilância (PRAC) da EMA encontra-se a fazer uma revisão dos dados sobre o risco de pensamentos suicidas e de auto-mutilação com a utilização de medicamentos agonistas do receptor GLP-1, incluindo Ozempic® e Wegovy® (semaglutida) e Saxenda® (liraglutida).
A revisão foi desencadeada pela agência de medicamentos Islandesa após relatos de pensamentos suicidas e automutilação em pessoas que usam medicamentos liraglutida e semaglutida. Até agora, foram reportados ás autoridades 150 casos de possíveis ocorrências de automutilação e pensamentos suicidas, que estão a ser analisados.
Os medicamentos liraglutida e semaglutida são amplamente utilizados, por mais de 20 milhões de pacientes/ano. Ainda está por esclarecer se os casos reportados se devem aos próprios medicamentos, às condições subjacentes dos pacientes ou a outros fatores.
Saxenda e Wegovy são autorizados para o controlo do peso, juntamente com dieta e atividade física em pessoas obesas ou com excesso de peso na presença de pelo menos um problema de saúde relacionado ao peso. Ozempic está autorizado para o tratamento de adultos com diabetes tipo 2 insuficientemente controlada como adjuvante de dieta e exercício, mas tem sido também usado off-label para perda de peso. O comportamento suicida não está atualmente descrito como efeito colateral nas informações do produto na UE para nenhum agonista do receptor GLP-1.
A revisão de Ozempic, Saxenda e Wegovy começou em julho de 2023 e agora foi alargada para incluir outros agonistas do receptor GLP-1, sendo que se prevê a sua conclusão em novembro de 2023.
Em Portugal, o semaglutido está aprovado para a terapêutica de diabetes tipo 2 mas não tem indicação terapêutica aprovada no tratamento da obesidade, ou excesso de peso, em doentes não diabéticos, pelo que a sua utilização nestas situações se trata de uma utilização off-label, que deverá ser discutida com o doente, e que tem levado ao aumento da despesa do Serviço Nacional de Saúde e causado ruturas no mercado e escassez nas farmácias, mesmo para os diabéticos, o que levou o Ministério da Saúde a tomar medidas de modo a limitar a sua prescrição.
Tal como acontece com todos os medicamentos, os doentes e os profissionais de saúde são aconselhados a utilizar agonistas dos recetores GLP-1 de acordo com as informações aprovadas do produto. Os pacientes e profissionais de saúde também devem relatar suspeitas de efeitos colaterais às autoridades. As informações sobre como notificar suspeitas de efeitos colaterais estão disponíveis nos folhetos informativos e nos sites das autoridades nacionais de medicamentos.